[시사뉴스 김성훈 기자] 코오롱생명과학의 골관절염 유전자 치료제 ‘인보사케이주’의 품목허가가 취소됐다. 2017년 7월 식약처로부터 품목허가를 받은지 1년 10개월만의 퇴출이다. 특히 악성종양의 원인이 될 수도 있어 인체사용을 금지한 세포를 사용한 것으로 알려져 그 후폭풍이 거세지고 있다.
식약처, 인보사 허가취소·형사고발
식품의약품안전처는 코오롱생명과학의 골관절염 유전자 치료제 '인보사케이주'(인보사)의 품목허가를 취소한다고 28일 밝혔다.
식약처는 28일 충북 오송 식약처 브리핑실에서 '코오롱생명과학 인보사 조사 결과' 브리핑을 열고 "인보사 2액이 허가 신청 당시 제출한 자료에 기재된 연골세포가 아닌 신장세포로 확인됐고, 코오롱생명과학이 제출했던 자료가 허위로 밝혀졌다"며 이같이 말했다.
인보사는 사람 연골에서 추출한 연골세포(HC)가 담긴 1액과 연골세포 성장인자(TGF-β1)를 도입한 형질전환세포(TC)가 담긴 2액을 3대1 비율로 섞어 관절강 내에 주사하는 세포 유전자 치료제다. 하지만 최근 2액 세포가 애초 식약처 허가를 받기 위해 코오롱생명과학이 제출한 자료에 기재된 '연골세포'가 아닌 '신장세포'(GP2-293세포)라는 것이 15년 만에 밝혀졌다.
식약처가 인보사 2액의 최초세포와 제조용세포 등에 대해 친자확인 검사인 유전학적 계통검사(STR)를 실시한 결과, 2액은 허가 당시 제출한 자료에 기재된 연골세포가 아닌 신장세포임이 확인됐다.
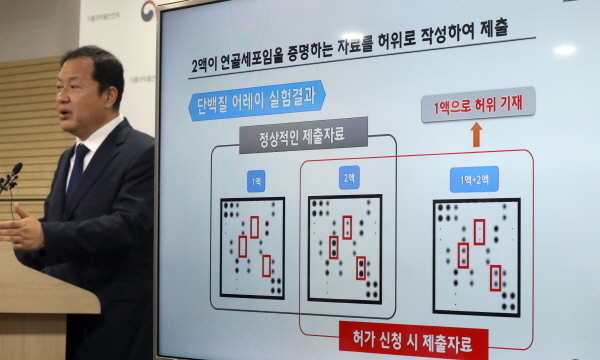
또 코오롱생명과학 국내 연구소를 조사한 결과, 허가 당시 제출한 자료 중 2액이 연골세포임을 증명하는 자료를 허위로 작성해 제출한 사실이 확인됐다. 식약처는 "2액이 1액과 같은 연골세포임을 증명하려면 ‘1액’과 ‘2액’의 단백질 발현 양상을 비교·분석해야 하는데, ‘1액과 2액의 혼합액’과 ‘2액’을 비교한 것으로 확인됐다"고 말했다.
이 뿐 아니다. 인보사를 개발한 코오롱생명과학의 자회사 미국 코오롱티슈진에 대한 현지실사 결과 코오롱생명과학은 허가 전 2액 세포에 삽입된 연골세포 성장인자 유전자의 개수와 위치가 변동된 사실을 알고도 이를 숨기고 관련 자료를 식약처에 제출하지 않은 것으로 드러났다.
식약처는 "조사 결과를 종합해 볼 때 코오롱생명과학이 인보사 허가를 위해 제출한 서류에 중대한 하자가 있는 것으로 확인됐다"며 "인보사에 대한 품목허가를 취소하고 코오롱생명과학을 형사고발하기로 했다"고 말했다.
식약처가 코오롱생명과학에 대한 검찰 수사를 의뢰하면서 코오롱그룹도 태풍의 영향권에 들게됐다. 업계 관계자는 "인보사는 이웅열 전 코오롱 그룹 회장이 직접 투자를 결정한 만큼 그룹도 검찰 수사의 영향권에 들 수 있다"고 말했다.
이에 대해 코오롱 측은 "현재로선 할 얘기가 없다. 상황을 예의주시하고 있다"며 말을 아꼈다.
피해자 단체 소송 제기
'인보사케이주'(인보사)를 투약한 환자들이 피해를 책임지라며 단체소송을 제기했다. 법무법인 오킴스는 지난 28일 코오롱 인보사 투약 환자 244명을 대신해 코오롱티슈진을 상대로 손해배상을 청구하는 소송 소장을 서울중앙지법에 냈다.
이들은 "이 사건 주사제에는 연골재생 효과가 없을 뿐만 아니라 오히려 악성 종양의 원인이 될 수 있어 인체에 사용을 금지한 세포가 포함돼 있다"며 "환자들은 자신의 의사와 무관하게 검증조차 되지 않아 언제 어떤 질병으로 발전될지 모르는 시한폭탄을 평생 안고 살아야 한다"고 주장했다. 청구금액은 1인당 1000만원씩 약 25억원이다. 향후 추가 손해를 입증해 청구취지를 확장할 예정이다.
이 소송을 대리하는 엄태섭 변호사는 "무엇보다 신장세포라는 건 전세계적으로 어떤 사람에게도 투약된 사례가 없고 우리 국민에게만 투약했다"며 "어떻게 질병으로 발현될지 모르는데 제거 방법이 명확하지 않다는 것만으로도 충분히 손해가 입증 가능하다고 생각한다"고 말했다.
오킴스 측은 추가 소송인단을 모집해 2차 소송을 접수할 계획이다. 지난 24일 기준 378명이 참여의사를 밝혔고 이 중에서 필요한 서류를 완비한 244명이 먼저 소송을 제기했다고 한다.
정부 뒤늦은 대책..첨단바이오 의약품 안전관리 강화
식약처는 인보사 사태를 계기로 내년부터 첨단바이오의약품에 대해 원료채취 단계부터 허가·생산, 허가 이후까지 안전관리를 강화하기로 했다.
보건복지부, 기획재정부, 과학기술정보통신부, 식품의약품안전처 등 관계 부처는 22일 충북 오송첨단의료산업진흥재단 C&V센터에서 이 같은 내용이 담긴 '바이오헬스 산업 혁신전략'을 발표했다.
식약처는 바이오 의약품 원료 채취와 관련해 '인체 세포 등 관리업' 제도를 신설해 인체 세포·조직 채취부터 수입, 처리, 보관에 이르기까지 별도 안전관리 기준을 마련할 예정이다.
개발과 제조에 사용한 모든 세포에 대해 유전학적 계통 검사를 의무화하는 등 강화한 허가·생산 관리 기준을 적용한다. 세포·유전자 치료제 등 첨단 바이오 의약품을 투여한 모든 환자를 대상으로 한 장기 추적 조사도 법적으로 의무화할 방침이다.
복지부와 식약처는 국회 법제사법위원회에 계류 중인 '첨단 재생 의료 및 첨단 바이오 의약품법'(첨단 바이오법) 제정에도 힘을 싣기로 했다.